身の回りの物質は混合物が多いということはお伝えしました。いろいろな用途で使えるようにするために、分離(分けて)・精製(純度をあげる)ということが必要になってきます。ろ過や蒸留ではその過程で注意点もありますのでここでお伝えします。
分離と精製
自然界に存在する普通に目にしたり触ったりする物質の多くは混合物です。
例えば、
空気、これは見えませんが窒素と酸素や他の微量な気体との混合物として存在しています。
水、これもほとんどは混合物です。
水道水も川の水も海水もいろいろな物質が混じっています。
飲んでいる水は純水ではありませんよ。
市販の水でもあるじゃないですか。
「ミネラル豊富な天然水」
とかって売っているでしょう?
「あ~、『水素水』とかある。」
って化学を勉強しているなら疑問に思って欲しいのですが、
水素って水にほとんど溶けないのですが、
「水素水って何?」
二酸化炭素は割と水に溶けるから炭酸水は分かるけど、
「水素水っていったい何よ?」
って疑問になりませんか?
化学を身近に感じるためにも、いろいろな疑問を持つことは良いことだと確信します。
別に化学の道に進む必要はないんですよ。
神経質にならなくても良いけど、普段の生活でも「?」と疑問に思うくらいしても良いのではないかな?
と感じているだけです。
いろいろなものが売られているので、
だまされて変なもの買わないくらいの疑問は持っても良いんじゃないかな。
余談が長くなりました。
化学に少しでも興味を持ってくれるといいなあ、という現れです。笑
そこで(どこで?),
混合物から目的とする純物質を取り出すことを分離といいます。
また,
取り出した物質から不純物を取り除いて,
より純度の高い物質を得ることを精製といいます。
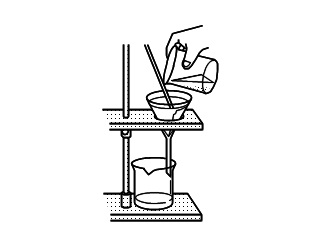
ろ過
液体とその液体に溶けない固体を分際する方法をろ過といいます。
ろ過を行うと、固体として存在している物質がろ紙上に残ります。
このときろ紙を通り抜けた液体を濾液といいます。
ろ過の注意点
ろ過の際の注意点です。
①
試科液はガラス棒を伝わらせて静かにそそぐこと。
(ろ過する液体が飛び跳ねないようにするため)
②
ろ紙は4つに折り,少量の水にぬらしてろうとに密着させること。
(ろ過する液体でぬらすという意味で水とは限らない)
③
試料液は.ろ紙の8分目以上入れないこと。
(入れすぎは良くない)
④
ろうとの先端は切り口の長いほうをビーカーの内壁につけておくこと。
(ろ液が絶え間なく流れ落ちろ過速度が大きくなる)
などがあげられます。
他にも、
ろ過する液体をあらかじめ静置して固体を沈殿させておけば、
最初、上澄み液からろ過し始めることでろ紙の目詰まりが減り、
ろ過時間を短縮することが出来ます。
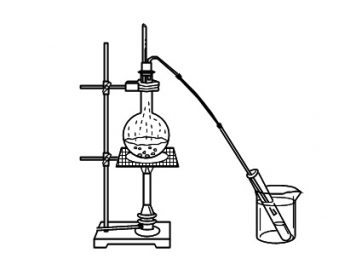
蒸留
液体の混合物を加熱して,
揮発性の成分を一度気体とし,
冷却後再び液体として分離する方法を蒸留(じょうりゅう)といいます。
例
食塩水(水+食塩〔溶液〕)から水(溶媒)だけを分離するのに用いる場合、
溶液(食塩水)を加熱すると水が気体(水蒸気)となって、
その気体だけを冷やして集めると純物質としての水が集められます。
蒸留の注意点
蒸留を行う場合の注意点です。
①
温度計の下端部を、枝付きフラスコの枝元の位置に合わせること。
(留出気体の温度が一定となり求める気体の沸点と一致していれば留出液は純物質と判断出来る)
②
液量はフラスコの2分の1以下にすること。
(あまり液が多いと沸騰するとき枝の方へ原液が流れ込む可能性がある)
③
突沸を防ぐために沸騰石を入れておくこと。
(沸騰石内の空気が気泡として発生し、突沸を防ぐことが出来る)
④冷却器を使う場合、
冷却水は下から上へ流れるようにすること。
(逆に流すと冷却器に水がたまらず、冷却効果が落ちる)
⑤
液を受ける受け器(三角フラスコなど)は密閉しないこと。
(加圧状態となり接合部がはずれたり破損する恐れがある)
などがあります。
ビーカーやフラスコに液体を入れて加熱するときは、
炎を直接あてると局所的に温度があがり器具の破損につながりますので注意して下さい。
加熱するときは水浴や油浴を利用し、
直接炎をあてて加熱しないという方法もありますよ。
物質の純度を上げるという操作は化学では重要なんですよ。