飽和炭化水素については「有機化合物の分類」でお伝えしてありますのでアルカンとシクロアルカンの具体的な説明に入りたいと思います。炭素数の少ない順にいくつか名前を覚えておいた方が良いものがありますので繰り返し見ておくと良いでしょう。
アルカンの名前と性質
炭素と炭素の結合がすべて単結合で構成されている鎖式の炭化水素をアルカンといいます。
最小構成単位となるのがメタンなのでメタン系炭化水素とも言います。
炭素原子の少ない順に
メタン \(\mathrm {CH_4}\)
エタン \(\mathrm {C_2H_6}\)
プロパン \(\mathrm {C_3H_8}\)
ブタン \(\mathrm {C_4H_{10}}\)
ペンタン \(\mathrm {C_5H_{12}}\)
ヘキサン \(\mathrm {C_6H_{14}}\)
ヘプタン \(\mathrm {C_7H_{16}}\)
オクタン \(\mathrm {C_8H_{18}}\)
ノナン \(\mathrm {C_{9}H_{20}}\)
デカン \(\mathrm {C_{10}H_{22}}\)
・・・
エイコサン \(\mathrm {C_{20}H_{42}}\)
(ギリシャ語の20「エイコサ」にアルカンにつく語尾aneがついたもの)
一般式は \(\mathrm {C_nH_{2n+2}}\) となります。
(一般式というのは炭素数を文字で \(\color{red}{n}\) としたときの分子式です。)
炭素数4のブタンまでは常温で気体で、ギリシャ語の数詞とは違う読み方になるので覚えておくしかありません。
ペンタンからデカンまでは常温で液体です。
アルカンはいってしまえば油です。
水に溶けにくく有機溶媒に解けやすい性質を持っています。
一般に分子量が大きいほど融点・沸点は高くなります。
ギリシャ語の数詞は物質の命名で良く使うので示しておきます。
1.モノ(mono)
2.ジ(di)
3.トリ(tri)
4.テトラ(tetra)
5.ペンタ(penta)
6.ヘキサ(hexa)
7.ヘプタ(hepta)
8.オクタ(octa)
9.ノナ(nona)
10.デカ(deca)
覚えおくと便利です。
アルカンの構造と命名法
アルカンはメタンが次々につながった分子構造をしています。
アルカン全体の立体的な構造は今のところ分からなくて良いですが、
メタンが「四面体構造」をしているということは覚えておいてください。
ちなみに、
メタンから水素が1つとれた原子団(基)をメチル基 \(\mathrm {CH_3-}\) といいます。
同じようにアルカンから水素が1つとれた基を「アルキル基」といいます。
アルカンの名前は鎖の一番長い部分(主鎖)が主な名前になります。
枝分かれしたアルキル基(側鎖)は主鎖についた炭素の何番目にあるかを示します。
このとき番号はできるだけ小さい数字となるように番号付けされます。
例えば、ブタンにメチル基をつけるとき一番端につけると主鎖が伸びてペンタンになります。
メチル基をブタンの2番目の炭素につけると、2-メチルブタンになります。
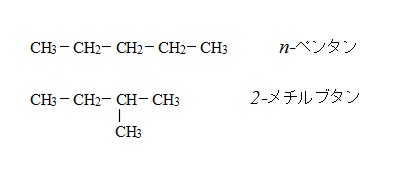
反対から見れば3番目の炭素についているように見えますが、2の位置の方が数字が小さくなるので「2-」と命名します。
命名法はもっと詳しく別のところで説明することにします。
アルカンの構造異性体
アルカンの炭素数が4以上の化合物は構造異性体が存在します。
ペンタンの構造異性体は

の3つとなりますが、炭素数が増えるにつれて構造異性体の数は増えていきますので注意しておきましょう。
構造異性体は分子の形状が変わりますので沸点や融点が異なります。
アルカンの反応性
アルカンは常温では酸、塩基、酸化還元剤とも反応しませんので反応性が良いとはいえませんが、特別な条件下では反応が起きます。
例えば、
光(紫外線)が存在する条件下ではアルカンはハロゲンと反応します。
メタンに塩素分子を加え光を当てるとメタンの水素と塩素が置き換わる「置換反応」が段階的に起こります。
\(\mathrm {CH_4} →(光、\mathrm {Cl_2})→ \mathrm {CH_3Cl}\)
クロロメタンが生成しました。次に、
\(\mathrm {CH_3Cl} →(光、\mathrm {Cl_2})→ \mathrm {CH_2Cl_2}\)
と、ジクロロメタンが生成し、
\(\mathrm {CH_2Cl_2} →(光、\mathrm {Cl_2})→ \mathrm {CHCl_3}\)
トリクロロメタン(クロロホルム)となります。
ついにはすべての水素が塩素に置き換わり、
\(\mathrm {CHCl_3} →(光、\mathrm {Cl_2})→ \mathrm {CCl_4}\)
テトラクロロメタンが生成します。
これらの反応は光によって起こるので少しやっかいな反応となりますが、
原子と原子が置換されているので「置換反応」であることは覚えておきましょう。
置換によって生成した物質は「置換体」というので一緒に覚えておくと良いですね。
シクロアルカン
環状構造をもつ飽和炭化水素をシクロアルカンといいます。
環状になる部分の炭素-炭素結合が鎖式のときより増えるので、
ついている水素の数は2つ少なくなります。
一般式は \(\mathrm {C_nH_2n}\) です。
シクロアルカンを考慮し出すと異性体の数はぐんと増えますので炭素の結合の仕方はしっかり理解しておく必要があります。
シクロプロパンには異性体はありませんが、炭素数が4以上になると異性体が存在しますので注意してください。
分子式だけを見るとシクロプロパンは「アルケン」と同じです。
分子式からの異性体の数はもっと増えますのでいろいろな場合を考えて構造式を書くようにしておきましょう。
次は不飽和結合を持つ炭化水素です。
アルカンとはセットでしっかり覚えておきましょう。