共有結合を図的に示す構造式とその書き方を紹介します。構造式は後々になりますが有機化学を学ぶときに非常に役に立ちます。分子の中で原子のつながり方を示すのでどういう仕組みで分子ができているか、どのような働きをもつ構造なのかが分かるようになりますよ。
構造式
共有結合の1組の共有電子対を1本の線で表して原子どうしの結合を表した式を構造式といいます。
そして構造式を表す線を価標と呼びます。
各原子から出る価標の数は原子の持つ不対電子対の数と等しくて、その数をその原子の原子価といいます。
例えば、
水素の価電子は1個で不対電子も一個ですので原子価は1価です。
フッ素の価電子は7個で6個は対になっているので不対電子は1個なのでフッ素の原子価も1価です。
酸素は価電子6個なので対になっている電子は4個で残り2個は不対電子となっていて原子価は2価です。
有機化合物の基本骨格となる炭素は価電子4個で不対電子は4個なので原子価は4価です。
原子価は周期表から価電子数が分かるので周期表を書いて考えると良いですね。
いろいろと書いていくと分かってきますが、原子価とは他の原子と何本手を伸ばして結合できるかという数です。
一番知っておいた方が良いのは炭素の4価です。
炭素は手が4つあると思っていてください。w
単結合・二重結合・三重結合
共有結合の種類ですが3種類です。
価標が1本で共有電子対1組の単結合。
例えば水素分子は2つの水素原子が単結合で結ばれています。\(\mathrm{H\color{red}{-}H}\)
価標が2本で共有電子対2組の二重結合。
例えば酸素分子は2つの酸素原子が二重結合で結ばれています。\(\mathrm{O\color{red}{=}O}\)
価標が3本で級友電子対3組の三重結合。
例えば窒素分子は2つの窒素原子が三重結合で結ばれています。\(\mathrm{N\color{red}{≡}N}\)
これらは2つの原子どうしでの結合を表していて、多数の原子と結合している数ではありませんので間違えないようにして下さい。
※
四重結合と言うものは存在しません。
上で示した例は2原子分子ですが原子がいくつになっても部分的にはこの3つの結合しかありません。
すべて単結合、二重結合、三重結合の組み合わせでできています。
構造式の書き方
原子価はその原子のもつ手の数だというのを先ほど書きましたが、構造式を書く場合はその手、原子価をすべて使うように組み合わせて書きます。
例えば水分子( \(\mathrm {H_2O}\) )は水素原子2個と酸素原子1個でできています。
これは水素の原子価は1でそれが2個あり、酸素の原子価は2でこの酸素の2つの手と水素原子2つが結びつくことですべての手を使うことになります。
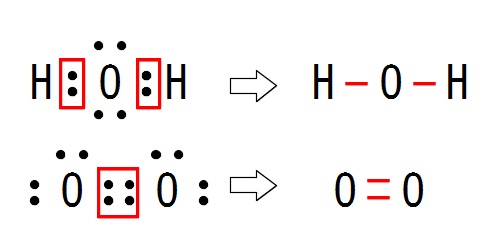
水の構造式は \(\mathrm{H-O-H}\) となります。
酸素が手2本、水素が手を1本ずつ出し切っていますので完了です。
共有電子対は価標で表しますが、非共有電子対は構造式では省略します。
本当は酸素と2つの水素の角度は直線ではありませんが構造式は立体的な構造まで示す必要はありません。
平面、直線を使って示せば十分です。
価標の長さも決まりはありません。
価電子の点と見分けられれば良いので「線です」と言える長さでいいでしょう。w
数学で等号(=)と比(:)を使い分けるくらいの違いですね。
もう一度まとめると、
「共有電子対は1組を価標1本で表し、非共有電子対は省略する。」
が基本です。
立体構造は示す必要はありませんが各原子の原子価である手の数、不対電子はすべて使いますから各原子の周りに電子が8個あるか確認しましょう。
共有結合は価電子8個になって各原子が安定するというのを忘れないでください。
構造式については有機化合物の分子の形を見る時にもっと理解が深まると思います。
価電子と不対電子をしっかり復習して、手の数を余らせないように線で結ぶと構造式ができると思っていて下さい。
有機化合物の構造式は
⇒ 有機化合物の官能基の種類と構造式の書き方
を参考にして下さい。
構造式を電子式に戻す方法
電子式よりも構造式の方が分子構造は分かり易いですが、基本は電子式にあるので構造式から電子式に戻す方法を書いておきます。
これは構造式の書き方の逆なのでむずかしくはありません。
先ず、価標(構造式の線です)1本を共有電子対1組に戻します。
その後各原子の価電子を8個にするように省略していた非共有電子対を書き足します。
ただし、水素は価電子が2個で閉殻するので8個ではありませんので注意して下さい。
ここだけでは構造式は理解できないと思うので、
⇒ 原子の電子配置 電子殻と電子数
や
⇒ 分子式と組成式との違いと共有結合の仕組みと電子式
で復習しておいて、
手を余らせないように結びつけることだけでもできるようになっておいてください。
単なる足し算なのでパズルみたいに組み合わせれば簡単です。w