アルコールの級数によってできてくる酸化物はアルデヒド、カルボン酸、ケトンと変わってきますので必ずチェックしておきましょう。アルコールの製法や性質から脱水反応などを見ていきましょう。アルコールの酸化や構造の変化によってできる誘導体は良く問題に出ます。
アルコールの製法
メタノールは一酸化炭素と水素の混合気体を高温高圧で反応させる工業的製法が用いられます。
\(\mathrm {CO} + \mathrm {2H_2} → \mathrm {CH_3OH}\)
このとき触媒には酸化亜鉛(\(\mathrm {ZnO}\))などが用いられ400℃くらいまで加熱します。
エタノールはエチレンに水を付加(高温の水蒸気を反応)させることで工業的につくられます。
\(\mathrm {CH_2=CH_2} + \mathrm {H_2O} → \mathrm {C_2H_5OH}\)
このときの触媒はリン酸(\(\mathrm {H_3PO_4}\))を用います。
エタノールはグルコース(ブドウ糖 \(\mathrm {C_6H_{12}O_6}\))を酵母などの菌を用いてアルコール発酵させることでも生成します。
\(\mathrm {C_6H_{12}O_6} → \mathrm {2C_2H_5OH} + \mathrm {2CO_2}\)
アルコールの性質
メタノールやエタノールを見れば分かりますが炭素数の少ないアルコールは常温で液体です。
ヒドロキシ基の分子全体に占める割合が大きいので水に良く溶けます。
アルコール( \(\mathrm {R-OH}\) )の \(\mathrm{R}\) の部分は炭素鎖で水と親和しない疎水性です。
親水性があるのはヒドロキシ基( \(\mathrm {OH}\) )部分なので炭素数の少ないアルコールは水に溶けやすいのです。
逆に炭素数が多くなると水に溶けにくくなります。
アルコールは金属ナトリウムを反応させると「ナトリウムアルコキシド」を生じて水素を発生します。
ナトリウムエトキシドの生成は下の反応式で示されます。
\(\mathrm {2C_2H_5OH} + \mathrm {2Na} → \mathrm {2C_2H_5O^-Na^+} + \mathrm {H_2}\)
ナトリウムアルコキシド( \(\mathrm {R-ONa}\) )は水酸化ナトリウムと同じ強塩基で、
この反応はアルコールのヒドロキシ基( \(\mathrm{OH}\) )の検出に用いられる反応です。
アルコールの脱水反応
アルコールに濃硫酸を加え加熱すると反応温度によってエーテルやアルケンを生じます。
例えばエタノールに濃硫酸を加え加熱すると反応温度によって、
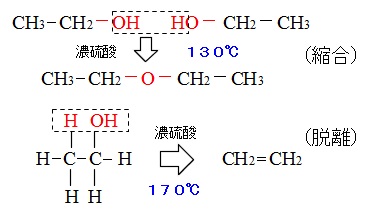
130℃前後で反応させると、(割と低めに設定すると)
エタノール2分子から水1分子とれる脱水縮合してジエチルエーテルを生成します。
\(\mathrm {2C_2H_5OH} → \mathrm {C_2H_5OC_2H_5} + \mathrm {H_2O}\)
170℃前後で反応させると、(高めの温度設定)
エタノール1分子から水1分子が脱離してエチレンを生成します。
\(\mathrm {C_2H_5OH} → \mathrm {CH_2=CH_2} + \mathrm {H_2O}\)
※
2分子から水がとれて結合する反応を「縮合反応」といい、
1分子から水がとれて2重結合ができる反応を「脱離反応」といいます。
また、ジエチルエーテルはナトリウムエトキシドにハロゲン化炭化水素を反応させても生成します。
\(\mathrm {C_2H_5ONa} + \mathrm {C_2H_5Cl} → \mathrm {C_2H_5OC_2H_5} + \mathrm {NaCl}\)
アルコールの酸化
アルコールを酸化剤を用いて酸化する第1級アルコールと第2級アルコールは違った物質を生成します。
第1級アルコールの酸化
第1級アルコールはヒドロキシ基がついている炭素に水素が2つあるのでアルデヒドを生成し、さらに酸化が進むとカルボン酸になります。
例えばエタノールを酸化するとアセトアルデヒドになり、さらに酸化すると酢酸になります。
\(\mathrm {C_2H_5OH} → \mathrm{CH_3CHO} + \mathrm{CH_3COOH}\)
第2級アルコールの酸化
第2級アルコールはヒドロキシ基がついている炭素に水素が1つなのでケトンとなります。
例えば2-プロパノールを酸化するとアセトンが生成します。
\(\mathrm {CH_3CH(CH_3)OH} → \mathrm{CH_3COCH_3}\)
第3級アルコールの酸化
第3級アルコールはヒドロキシ基がついておる炭素に抜けていく水素がないので酸化されません。
アルコールの酸化が進むには炭素と酸素の二重結合ができるために、
ヒドロキシ基がついた炭素に抜けていく水素が無いとダメだという見方で良いです。
第三級アルコールは無理矢理酸化することもできますが、炭素-炭素結合が切れるほどのエネルギーが必要です。
「酸化されにくい」というのが本当なのですが今のところ「酸化されない」と考えていていいでしょう。
これからエーテルやカルボン酸について詳しく見ていくことになります。
官能基は何度も見て覚えておきましょう。
同じ酸素を介した結合でも性質は全く違ってきます。