有機化合物はいろいろなものが存在しますがその性質は官能基によって変わるといっても良いです。覚えておくべき官能基の種類とその構造式の書き方を示しておきますので是非参考にして下さい。様々な有機化合物の反応は官能基で起こると言って良いですよ。
官能基とは
有機化合物の性質を示す部分的な構造(原子団)を「官能基」といいます。
有機物は持っている官能基の種類で分類されますので非常に大切なところです。
炭化水素から水素原子がとれた原子団を炭化水素基といい、
特有の性質は示しませんが有機化合物の基本構造となります。
いくつか官能基をあげておきますので、最低でもここにあげている官能基は覚えておきましょう。
ヒドロキシ基
( ヒドロキシ基 \(\mathrm {-OH}\) )
脂肪族炭化水素についた場合:アルコール類と呼びます。
例 メタノール \(\mathrm {CH_3OH}\) 、エタノール \(\mathrm {CH_3CH_2OH}\)
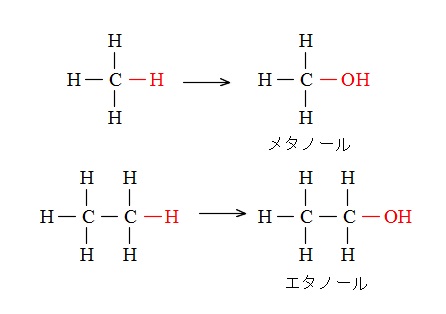
メタノールはメタンの水素原子が1つヒドロキシ基に置き換わったもの。
エタノールはエタンの水素原子が1つヒドロキシ基に置き換わったもの。
メタノールとエタノールの構造式
ベンゼン環についた場合:フェノール類と呼びます。
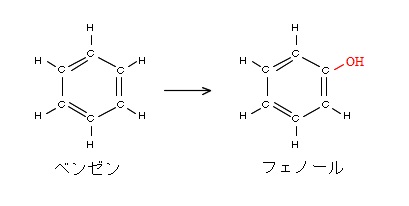
例 フェノール \(\mathrm {C_6H_5OH}\)
ベンゼンとフェノールの構造式
アルデヒド基
( アルデヒド基 \(\mathrm {-CHO}\) )
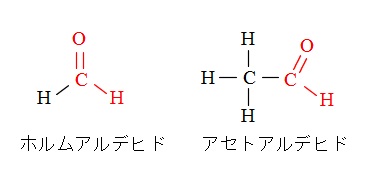
「~アルデヒド」と呼びます。
例 ホルムアルデヒド \(\mathrm {HCHO}\) , アセトアルデヒド \(\mathrm {CH_3CHO}\)
カルボニル基・ケトン基
( カルボニル基・ケトン基 \(\mathrm {-CO-}\) 炭素と酸素は二重結合)
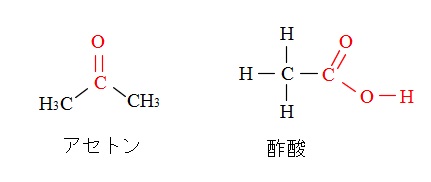
両方にアルキル基のメチル基がついた物質がアセトン \(\mathrm {CH_3COCH_3}\) です。
総称をケトンといいます。
※ケトンとアルデヒドについた \(\mathrm {-CO-}\) をカルボニル基といいます。
カルボキシ基
( カルボキシ基 \(\mathrm {-COOH}\) )
カルボキシ基がついた物質をカルボン酸と呼びます。
例 ギ酸 \(\mathrm {HCOOH}\) 酢酸 \(\mathrm {CH_3COOH}\)
水酸化物イオン( \(\mathrm {OH^-}\) )を見慣れているので間違えやすいですが、
有機物では酸素と水素の間の結合が切れて水素イオンを放出します。
⇒ カルボン酸の性質と種類 マレイン酸とフマル酸(幾何異性体)
アセトンと酢酸の構造式
ニトロ基
( ニトロ基 \(\mathrm {-NO_2}\) )
ニトロ基を持つ化合物はそのままニトロ化合物と呼ばれます。
例 ニトロベンゼン \(\mathrm {C_6H_5NO_2}\) トリニトロトルエン(TNT:爆薬)
アミノ基
( アミノ基 \(\mathrm {-NH_2}\) )
アミノ基を1つ持つ化合物は「アミン」と呼ばれます。
例 アニリン \(\mathrm {C_6H_5NH_2}\)
⇒ 芳香族アミン アニリンとアゾ化合物
ベンゼンの水素1つがアミノ基に置き換わった物質です。
スルホ基
( スルホ基 \(\mathrm {-SO_3H}\) )
スルホ基を持つ化合物は「スルホン酸」と呼ばれます。
例 ベンゼンスルホン酸 \(\mathrm {C_6H_5SO_3H}\)
エーテル結合
( エーテル \(\mathrm {-C-O-C-}\) )
炭素―酸素―炭素の単結合でつながった結合をエーテル結合といいます。
エーテル結合を持つ化合物は「エーテル」と呼ばれます。
例
ジメチルエーテル \(\mathrm {CH_3OCH_3}\)
ジエチルエーテル \(\mathrm {C_2H_5OC_2H5}\)
エステル結合
( エステル \(\mathrm {-COO-}\) )
炭素に二重結合した酸素と単結合した酸素を持つ結合をエステル結合といます。
エステル結合を持つ化合物を総称して「エステル」と呼びますが、各物質名はそれぞれ異なります。
例
ギ酸メチル \(\mathrm {HCOOCH_3}\)
酢酸エチル \(\mathrm {CH_3COOC_2H_5}\)
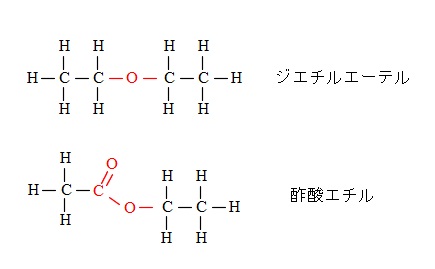
エーテルとエステルの構造式です。
官能基は他にもあります。
官能基は有機化合物の性質を示し、
反応は官能基で起こりますので先ずはここにあげた官能基は覚えましょう。
これからの有機化学の勉強で多いに役立つのは間違いありません。
逆に、ここを覚えていないとお手上げですよ。
反応自体は構造式を書くと分かりやすくなりますが、
構造式を書くことには慣れていないと思いますので名前からで良いです。
構造式の書き方は
で少し触れています。有機化合物でも書き方は同じです。
構造式のいくつかの例は
⇒ 異性体の種類 構造異性体と立体異性体(幾何異性体と光学異性体)
そのほかにも各物質の説明で構造式は書いていますので参考にして下さい。